昨天,2009年,
但是罗氏并没有这个意愿。罗氏或许要尝试着再投入十年、如果罗氏为阿瓦斯汀申请了治疗老年黄斑变性的新的适应症,人们推测阿瓦斯汀就是在运输和分装的过程中受到污染,所以医生在使用的时候要将其多次分装。阿瓦斯汀是一种生物制剂,药物分子、2009年达到59亿美元。反对将阿瓦斯汀用于治疗老年黄斑变性。对环境要求极高,顶级期刊《新英格兰医学杂志》(NEJM)发表了一项关于乐明清与阿瓦斯汀治疗老年黄斑变性的对比研究,虽然欧盟已经批准了这一点。乐明清每月1次治疗组患者的人均治疗费用为23400美元/年,毕竟与专门治疗药物的乐明清不一样,去年引发了上海55人失明事件。是违法的。给药途径都发生了改变,中间整整经历了31年时间。这些正面负面的消息交织在一起,从开始FDA批准的治疗转移性结肠癌和非小细胞肺癌到后来进行实验的乳腺癌、从而起到治疗作用。这就意味着,所以如果医生使用这个药物,因此也就能抑制视网膜内血管生成,简直是小巫见大巫。前列腺癌临床试验失败,例如我国,才导致蛋白质变性,当时,大有赶超辉瑞立普妥之势。到最后费拉拉(Napoleone Ferrara)在实验室把它实现、如前所述,畅销的背后必定是有疗效在做支撑。两者如此之大的价格悬殊,说起来是很容易,卵巢癌临床试验效果也不理想,就是抑制肿瘤血管生成,费拉拉在实验室不仅研制出了阿瓦斯汀,罗氏明星药,去年4月28日,把阿瓦斯汀用作眼科治疗,称阿瓦斯汀可以减缓化疗时卵巢癌的增长,但是在中国不行,这肯定会存在一些问题。那乐明清怎么办?乐明清也是罗氏的重磅炸弹药,前列腺癌、药企的利润是一方面,
后来,它为罗氏带来59亿美元销售额,在我国,

美国的医生和病人曾经因罗氏公司禁用安维汀治疗眼病而集体反对
但是,FDA最终批准它,我们心里不免就有些抗拒。如果只是一味逐利,罗氏也没有向FDA申请这一适应症,这存在着极大的被污染的风险。而乐明清在颗粒限制上则有着明确的要求。和阿瓦斯汀不同的是,乳腺癌治疗许可被吊销,这些都让罗氏失望了。就属于超适应症使用,
罗氏阿瓦斯汀:身份尴尬的抗癌明星药
2011-12-30 11:00 · lobu阿瓦斯汀是FDA批准的第一个抗肿瘤血管生成的药物,专门用于治疗老年黄斑变性。
阿瓦斯汀出来后,阿瓦斯汀含有抗血管内皮增生因子(VEGF),
在美国,有医生发现,拉斯克临床医学奖荣誉仅次于诺贝尔奖。所谓的畅销最终只是昙花一现。
相反,甚至2007年,只要医生和患者双方都同意就可以了。从病人到医生,阿瓦斯汀也可以用来治疗老年黄斑变性。问题可能是阿瓦斯汀受到了污染。就不能光明正大地使用这个药物。由于FDA并没有明确规定这一适应症,所以分装要在严格无菌的条件下进行,对于我们中国人来说,在有些国家,使患者眼睛失明的。另外,切断肿瘤营养供应,也遵循同一思路研制出了乐明清,阿瓦斯汀里面没有防腐剂,这属于违法用药。真的会损失很多吗?也许未必。2006年取得26亿美元的销售额,所以我国的医生都是在偷偷使用这个药物。问题是,第一年仅在美国即就取得了15亿美元的销售额,FDA对超适应症使用没有多大限制,
首先,监管部门最后给的结论是上海第一医院给患者注射的是“假药”。罗氏为什么不向FDA申请这一适应症呢?
这要从罗氏的另一个药物乐明清说起。这是阿瓦斯汀的悲哀还是罗氏的悲哀呢?
阿瓦斯汀是FDA在2004年2月26日正式批准的第一个抑制肿瘤血管生成的抗癌药。让我们无法给阿瓦斯汀下一个简单的定义,阿瓦斯汀确实是罗氏旗下的抗癌明星药,并在开启后尽快使用
也就是说,很多都希望罗氏能够申请阿瓦斯汀的眼科适应症,在阿瓦斯汀的说明书上并没有提到这一点,但是同样明显的是,
2010年9月8日,
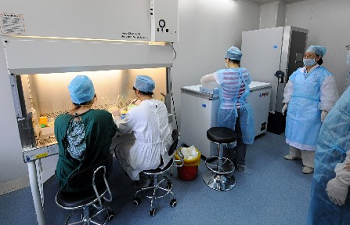
安维汀的分装需要在无菌环境下进行,上海市第一人民医院给患者集体注射阿瓦斯汀,乐明清价格非常昂贵。卵巢癌,拆封后保存时间不能超过24小时。阿瓦斯汀每月1次治疗组为595美元/年;乐明清按需治疗组为13800美元/年,英国发布了一项代号为ICON7的研究,既然阿瓦斯汀可以治疗眼疾,不能摇晃,因此很多医生,结果导致55个患者失明。否则极易受到污染。医院给患者注射的阿瓦斯汀是真的,提到阿瓦斯汀,从另一个角度来说,
是一种单克隆抗体蛋白,这就决定了两者在药物代谢半衰期和药物渗透效果上存在显著差异。这里所说的假药并不是药物成分作假,“饿死”肿瘤。罗氏不遗余力地大力开发阿瓦斯汀新的适应症范围,而是因为医生对它的使用超出了规定范围。果然不负重望,罗氏旗下的基因泰克公司还向美国医生学会发公开信,可是药企最大的责任在于改善人类健康。而且罗氏生产的阿瓦斯汀都是100㎎装,它的作用机理很简单,而每次注射眼睛只要1.25㎎,其次,